一、試驗儀器:ZDJ-4B型自動電位滴定儀
試驗
電極:E201-C型復合pH
電極
滴定方法:預設終點滴定.
二、溶劑配制:
0.1 mol/L鹽酸(HCL);
0.1 mol/L氫氧化鈉(NaOH);
8%甲醛溶液;
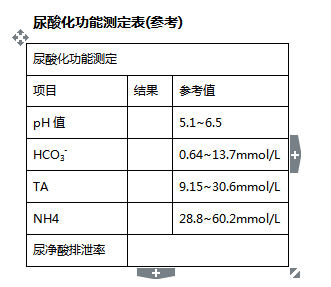
數據診斷:pH參考值5.1~6.5;
HCO
3- 濃度參考值0.64~13.7mmol/L。
三、實驗步驟:
1)儀器設置:滴定類型參數:pH滴定
終點數量:1個終點。終點參數(五個參數量,即終點pH值、預控點pH值、預控開關、預控量大小、終點延時時間)。
2)實驗步驟:
1. 取樣尿樣
20 mL。
2. 測量pH值:用滴定儀測量尿樣 pH值,并記錄尿樣初始 pH值。設pH 6.5。
3. 尿樣處理:加入0.1 mol/ HCL(鹽酸)5mL,加熱到 100 ℃,保持 15 分鐘。冷卻**室溫。
4. 空白試驗:取20mL去離子水,加入0.1mol/L HCL(鹽酸)5mL,用0.1 mol/L氫氧化鈉(NaOH)滴定直到pH為6.5。記錄耗去的氫氧化鈉溶液mL數。
5. **次滴定:應滴定到尿樣初始pH值為6.5,記錄耗去的氫氧化鈉溶液 x mL。
6. 第二次滴定:應滴定pH為7.4,記錄耗去的氫氧化鈉溶液 y mL 。
7. 加入10mL甲醛(8%)。第三次滴定:再滴定到pH為7.4,記錄耗去的氫氧化鈉溶液 z mL 。
四、結論:
1. 可以通過改變參數值(預控量大小,預控點)和增加來氫氧化鈉濃度縮短分析時間,
2. 滴定過程清洗要關注;可考慮純凈水清洗。
鄰氨基苯甲酸含量測定
一、 方法原理
鄰氨基苯甲酸含量測定:取本品約180mg,精密稱定,溶解在50ml 96%酒精中,混合物在攪拌下,用0.1mol/L的氫氧化鈉溶液滴定**終點。每1ml氫氧化鈉滴定液(0.1mol/L)相當于13.714mg的鄰氨基苯甲酸。
二、 實驗儀器及推薦配置
雷磁自動電位滴定儀
231-01 pH玻璃
電極 232-01參比電極
三、 實驗試劑
1、滴定液:0.1mol/L氫氧化鈉溶液配制
稱取4.000克分析純的氫氧化鈉,溶解于去離子水中,移入1000ml容量瓶中,并用水稀釋**刻度,搖勻。
2、基準純鄰苯二甲酸氫鉀:在105℃干燥**恒重
3、樣品
四、 樣品分析及結果計算
1、 標定
取在105℃干燥**恒重的基準鄰苯二甲酸氫鉀約0.6g,精密稱定,加新沸過的冷水50ml,振搖,使其盡量溶解。在自動電位滴定儀上滴定**終點,每1ml氫氧化鈉滴定液(0.1mol/L)相當于20.42mg的鄰苯二甲酸氫鉀。
按下列公式計算
CNaOH=0.1(
m鄰苯二甲酸氫鉀/0.02042)/
VNaOH
0.1 - 氫氧化鈉標準溶液理論濃度(mol/L)
C
NaOH – 氫氧化鈉標準溶液濃度(mol/L)
V
NaOH - 滴定**終點時消耗氫氧化鈉的體積(ml)
m
鄰苯二甲酸氫鉀 - 稱取的鄰苯二甲酸氫鉀質量(g)
0.02042 - 與1.00ml氫氧化鈉標準溶液[c(NaOH)0.1mol/L]相當的鄰苯二甲酸氫鉀的質量(g)
2、樣品分析
取本品約180mg,精密稱定,溶解在50ml 96%酒精中,混合物在攪拌下,用0.1mol/L的氫氧化鈉溶液滴定**終點。
按下列公式計算
鄰氨基苯甲酸含量=
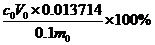
0.1 – 氫氧化鈉標準溶液理論當量濃度(mol/L)
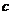 0
0 – 氫氧化鈉標準溶液實際標稱濃度(mol/L)
V
0 - 滴定突躍點時消耗氫氧化鈉的體積(ml)
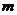 0
0 - 樣品質量(g)
0.013714 - 與1.00ml氫氧化鈉標準溶液[c(NaOH)0.1mol/L]相當的鄰氨基苯甲酸的質量(g)
結果(譜圖)
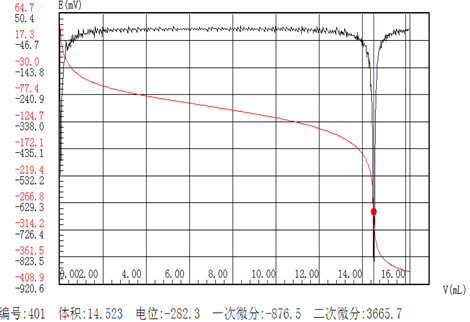
五、 結論與建議
參比電極內充液更換為非水溶劑的氯化鉀或氯化鋰飽和溶液,分析效果較好。

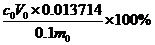
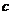 0 – 氫氧化鈉標準溶液實際標稱濃度(mol/L)
0 – 氫氧化鈉標準溶液實際標稱濃度(mol/L)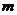 0 - 樣品質量(g)
0 - 樣品質量(g)